药物动态 第8期

为进一步规范β内酰胺类抗菌药物皮肤试验的使用和判读,促进抗菌药物合理应用,国家卫健委委托国家卫生健康委抗菌药物临床应用与细菌耐药评价专家委员会制定了《β内酰胺类抗菌药物皮肤试验指导原则(2021年版)》,于2021年4月13日发布。
β内酰胺类抗菌药物皮肤试验指导原则
(2021年版)
β内酰胺类抗菌药物是目前临床应用最多且具有重要临床价值的一类抗菌药物。由于医务人员对该类药物诱发过敏反应存在担忧,青霉素和头孢菌素皮肤试验被广泛应用于用药前预测过敏反应。然而,因为对药物过敏反应机制、皮试意义的认识误区,许多医务人员在临床实践中过于依赖皮试,过敏史甄别欠细致、皮试适应证偏宽泛、皮试操作不规范、结果判读不正确等现象仍普遍存在。由此可能导致过敏反应急救应对不足,浪费医疗资源,延误患者治疗,缩窄抗菌药物选择范围等后果。基于当前存在的问题和皮试的重要影响,为澄清药物过敏反应机制和皮试的临床意义,规范β内酰胺类抗菌药物过敏史甄别和皮试临床实践,保障患者安全,促进抗菌药物合理应用,特制定本指导原则。
一、皮肤试验及其诊断价值
皮肤试验包括点刺试验和皮内试验,目前国内抗菌药物皮肤试验常规采用皮内试验。以下提到的皮肤试验均指皮内试验,简称皮试。
(一)药物过敏反应与皮试的预测作用。
药物过敏反应根据免疫机制的不同分为Ⅰ、Ⅱ、Ⅲ、Ⅳ四型。Ⅰ型为IgE介导的速发型过敏反应,通常在给药后数分钟到1小时之内发生,典型临床表现为荨麻疹、血管神经性水肿、支气管痉挛、过敏性休克等。Ⅱ型为抗体介导的溶靶细胞过程,例如药物诱发的血小板减少性紫癜。Ⅲ型为免疫复合物介导,例如血清病、药物相关性血管炎等。Ⅳ型为T细胞介导,例如药物接触性皮炎、固定性药疹、Stevens/Johnson综合征、中毒性表皮坏死松解症等。Ⅱ、Ⅲ、Ⅳ型为非IgE介导的迟发型过敏反应,通常在给药1小时之后直至数天发生。
β内酰胺类抗菌药物皮试的主要目的,是通过检测患者体内是否有针对该类药物及其代谢、降解产物的特异性IgE抗体(specific IgE, sIgE),预测发生Ⅰ型(速发型)过敏反应的可能性,降低发生过敏性休克等严重过敏反应风险。预测Ⅱ、Ⅲ、Ⅳ型过敏反应不是皮试的目的,皮试也无法检测药品中是否含有杂质成分。
(二)青霉素皮试。
青霉素本身的分子量小,为半抗原,其代谢、降解产物与蛋白质或多肽结合形成可引发过敏反应的完全抗原。青霉素的β内酰胺环开环形成的青霉噻唑基,占其分解产物大多数,被称为主要抗原决定簇,其相应的批准上市皮试试剂由青霉噻唑基与多聚赖氨酸共价结合制备而成,称为青霉噻唑酰多聚赖氨酸(penicilloyl-poly-lysine,PPL)。青霉素还可形成其他降解物、重排物或降解中间体,例如青霉酸、青霉噻唑酸、脱羧青霉噻唑酸、青霉烯酸、青霉胺等。这些分解产物量少,构成次要抗原决定簇,其批准上市皮试试剂包括青霉酸、脱羧青霉噻唑酸等次要抗原决定簇混合物(minor determinant mixture,MDM)。青霉素G本身亦可归为次要抗原决定簇。所谓的“主要”和“次要”是指两类分解产物量上的差异,两者免疫学及临床重要性等同。国内目前暂无已批准上市的PPL及MDM试剂。此外,半合成青霉素侧链结构也可成为抗原决定簇,诱发过敏反应。
青霉素皮试是目前预测青霉素速发型过敏反应最快速、灵敏、有效的检测方法。完整的青霉素皮试,其检测试剂应包含青霉素G、MDM、PPL、半合成青霉素,并做阴性对照(生理盐水)及阳性对照(组胺)。研究表明,通过完整、规范的皮试诊断方法,青霉素皮试的阳性预测值为50%,阴性预测值为70%~97%。
(三)头孢菌素皮试。
头孢菌素分解产物尚未完全明确,但现有的证据表明头孢菌素类的抗原决定簇主要由其侧链结构所构成。头孢菌素之间的交叉过敏性可能主要是由于具有相同或相似的C7位的R1侧链(见附表)。迄今尚无批准上市的头孢菌素皮试试剂,且皮试的灵敏度、特异度、阳性预测值及阴性预测值亦未确定。
(四)青霉素与头孢菌素的交叉过敏反应。
青霉素与第一代头孢菌素之间的交叉过敏性较多见,可达10%。但第二代头孢菌素与青霉素之间的交叉过敏反应率仅为2%~3%,第三、四代头孢菌素与青霉素之间的交叉过敏反应率更低至0.17%~0.7%。目前研究认为头孢菌素C7位的R1侧链与青霉素C6位的侧链结构相同或相似是导致交叉过敏反应的主要因素(见附表)。
二、皮试适应证
使用β内酰胺类抗菌药物前是否需要进行皮试,由医师基于以下适应证判定。需进行皮试者,应由医师开具皮试医嘱后进行。
(一)青霉素类。
目前我国青霉素类抗菌药物说明书、《抗菌药物临床应用指导原则》和《中华人民共和国药典临床用药须知》均要求在使用青霉素类抗菌药物之前需常规做青霉素皮试。
(二)头孢菌素类。
头孢菌素给药前常规皮试对过敏反应的临床预测价值无充分循证医学证据支持,大多数头孢菌素类抗菌药物的说明书、《抗菌药物临床应用指导原则》和《中华人民共和国药典临床用药须知》均未要求头孢菌素用药前常规进行皮试。
不推荐在使用头孢菌素前常规进行皮试,仅以下情况需要皮试:①既往有明确的青霉素或头孢菌素Ⅰ型(速发型)过敏史患者。此类患者如临床确有必要使用头孢菌素,并具有专业人员、急救条件,在获得患者知情同意后,选用与过敏药物侧链不同的头孢菌素(见附表)进行皮试,其结果具有一定的参考价值;②药品说明书中规定需进行皮试的。应当向药品提供者进一步了解药品引发过敏反应的机理,皮试的灵敏度、特异度、阳性预测值和阴性预测值,并要求提供相应皮试试剂。
有过敏性疾病病史,如过敏性鼻炎、过敏性哮喘、特应性皮炎、食物过敏和其他药物(非β内酰胺类抗菌药物)过敏,发生头孢菌素过敏的几率并不高于普通人群,应用头孢菌素前也无需常规进行皮试。但上述患者用药后一旦出现过敏反应,症状可能会更重,应加强用药后观察。
(三)其他β内酰胺类。
青霉素类、头孢菌素类的β内酰胺酶抑制剂复方制剂,皮试适应证和方法可分别参照青霉素类、头孢菌素类药物。
单环类、头霉素类、氧头孢烯类、碳青霉烯类、青霉烯类等其他β内酰胺类抗菌药物均无循证医学证据支持皮试预测作用,给药前无需常规进行皮试。若这些类别药物的说明书要求使用前皮试,参照头孢菌素类处理。氨曲南侧链结构与头孢他啶C7位侧链结构相同,研究报道二者之间存在交叉过敏,有明确头孢他啶过敏史患者应避免使用氨曲南。
三、皮试操作基本原则与结果判读
(一)皮试液配制。
青霉素皮试液配制:根据《中华人民共和国药典临床用药须知》规定,以注射用青霉素G或青霉素G皮试制剂稀释为500U/ml的皮试液。前者需多步稀释;后者仅一步稀释,可节约操作时间和人力,并减少误差及污染。
头孢菌素皮试液配制:头孢菌素皮试不引发皮肤非特异性刺激反应的推荐浓度为2mg/ml。若确需进行皮试,需将拟使用的头孢菌素加生理盐水稀释至2mg/ml浓度配制成皮试液。
设立阴性对照(生理盐水)及阳性对照(0.01mg/ml磷酸组胺),有助于排除假阳性反应及假阴性反应。
(二)皮试操作方法。
用75%乙醇消毒前臂掌侧下段皮肤,对乙醇敏感的患者可使用生理盐水清洁。使用1ml一次性注射器抽取皮试液,先排净针管内空气。用一手绷紧患者皮肤,另一手持针,针头斜面向上,与皮肤呈5~15°进针,皮内注射皮试液0.02~0.03ml,形成直径3mm的皮丘。
(三)皮试结果的判断与解读。
进行皮试后15~20分钟后判断皮试结果,如皮丘较之前注射形成的皮丘直径扩大≥3mm应判断为皮试阳性,伴有红晕或痒感更支持呈阳性反应。
在排除假阳性反应的前提下,皮试阳性有临床意义,提示患者有发生IgE介导的速发型过敏反应的可能。皮试阳性(除非皮试诱发严重过敏反应)不应记录为“过敏”,而应记录为“皮试阳性”。既往仅皮试阳性的患者,并非皮试的禁忌证,可在密切观察基础上重复皮试。
皮试阴性不能完全排除过敏反应的可能,原因在于:①皮试仅对IgE介导的速发型过敏反应有预测价值,对非IgE介导的迟发型过敏反应无预测价值;②我国青霉素皮试检测试剂仅含青霉素G,部分医院加入了半合成青霉素,但未包含PPL、MDM,皮试的灵敏度有限;③未常规采用阳性对照,不能排除假阴性结果。因此即使皮试为阴性,在药物使用过程中仍需注意密切观察,并做好过敏反应抢救准备。
(四)皮试注意事项。
1.皮试有诱发严重过敏反应甚至过敏性休克的可能,皮试区应常规备有相关抢救设备及药品,且相关人员应接受过严重过敏反应抢救的正规培训;4~6周内发生过β内酰胺类药物严重过敏反应的患者进行皮试,由于sIgE在严重过敏反应发生时已被大量消耗,皮试可能出现假阴性结果。如需进行皮试,建议在反应发生4~6周后进行。
2.有些药物可抑制皮肤反应,导致假阴性结果,故皮试前应询问近期用药史,并在病情允许时停用可能干扰皮试结果的药物。全身应用一代抗组胺药物停药至少2~3天,二代抗组胺药物停药至少3~7天,全身较长时间应用糖皮质激素停药至少7天,丙咪嗪类抗抑郁药、吩噻嗪类抗精神病药停药至少7天,对皮试的影响才能消除。如用药史不明,或因客观原因无法停药或停药足够长时间,应以磷酸组胺作为阳性对照,明确皮肤反应性是否受抑制而导致假阴性。
3.哮喘控制不佳或哮喘急性发作期患者进行皮试,一旦出现严重过敏反应,症状会更重,因此皮试最好在哮喘控制期进行;若必须在非控制期进行皮试,需加强监测。
4.β受体阻滞剂及血管紧张素转化酶抑制剂可影响对严重过敏反应的救治。有严重过敏反应高危因素的患者,皮试前应至少停此类药物24小时。
5.皮试液浓度过高会引起皮肤非特异性刺激,操作者手法较重、注射量大及注入气泡等均可导致假阳性反应。
6.皮肤反应性增高(如部分荨麻疹、皮肤肥大细胞增多症)的患者可出现假阳性反应,影响结果判读,应以生理盐水作为阴性对照。
7.婴幼儿及老年患者皮肤反应性差,可能出现假阴性结果。
8.皮试液抗原性低或失效可导致假阴性反应,因此皮试液应尽量现配现用,如需保存应4℃冷藏,且保存时间不应超过24小时。
四、过敏史的甄别与严重过敏反应的救治
皮试仅为预防过敏反应的措施之一,其预测作用仅限于少数药物引发的IgE介导的速发型过敏反应。预防和降低过敏反应风险应更多依靠:
①详细询问和甄别过敏史;
②用药期间的密切观察;
③配备过敏反应抢救药品和设备;
④医务人员熟悉严重过敏反应救治措施。
采集和甄别过敏史,应认真询问并详细记录:
①可疑药物品种;
②给药途径;
③给药与出现疑似过敏反应的时间间隔;
④临床表现;
⑤处置与转归;
⑥经治医师所做诊断。
应注意鉴别患者所诉的“过敏反应”是否为非过敏性的药物不良反应。如考虑过敏反应,还应尽量区分为速发型还是迟发型。记录过敏史时,尽量具体到药物品种而非笼统表述为某类药物过敏;既往仅皮试阳性患者,应为“既往皮试阳性”,而不应表述为“过敏”。
严重过敏反应的抢救必须争分夺秒,救治的首要目的是维持有效通气及循环。抢救的首选用药是肾上腺素。糖皮质激素及抗组胺药物并不是严重过敏反应的抢救首选用药。糖皮质激素起效慢,对于严重过敏反应急性期无效,仅适用于预防严重过敏反应迟发相反应(少数患者严重过敏反应可为双相,即速发相反应消失4~8小时后症状再次出现,称为迟发相反应)。严重过敏反应的救治措施包括:①立即停用导致过敏药物,静脉给药者更换输液瓶及输液器,救治过程严密监控心率、血压、呼吸及血氧饱和度;②肾上腺素(1:1000):14岁及以上患者单次0.3~0.5ml深部肌内注射,14岁以下患者0.01ml/kg体重深部肌内注射(单次最大剂量0.3ml),5~15分钟后效果不理想者可重复注射,注射最佳部位为大腿中部外侧;③保持气道通畅,吸氧,必要时气管插管或气管切开,如暂无条件建立人工气道,紧急情况下可先行环甲膜穿刺;④建立静脉通道(两条或两条以上),静滴晶体液维持血压(液体用量20ml/kg,根据患者情况调整剂量),必要时静脉点滴多巴胺维持血压;⑤若有支气管痉挛,可吸入β2受体激动剂;⑥抗组胺药:如苯海拉明1.25mg/kg,最大量50mg,肌内注射;⑦糖皮质激素:静脉甲泼尼龙40mg/100ml生理盐水,或氢化可的松琥珀酸钠100mg~200mg;⑧任一环节中如出现心跳呼吸骤停,立即就地进行规范心肺复苏术。患者经救治脱离危险后,应留院观察至少12小时。
五、改进皮试实践的策略和措施
各级卫生健康行政部门、医疗机构和相关学术组织应充分认识规范β内酰胺类抗菌药物皮试对于抗菌药物合理应用的重大意义,基于当前实际,循序渐进地改进β内酰胺类抗菌药物皮试。
(一)积极组织医务人员进行有关β内酰胺类抗菌药物皮试适应证、意义、结果解读和过敏反应预防、救治的培训,纠正将预防过敏反应全部寄托于皮试、皮试适应证过泛的错误观念和做法。对从事皮试操作的护士进行过敏反应相关理论和皮试操作实践的重点培训。在有条件的医疗机构建立变态反应科,以提高皮试和过敏反应防控水平。
(二)各级卫生健康行政部门、医疗机构、相关学术组织等,应根据循证证据和本指导原则精神,修正相关规章、制度、指南、共识、专业著作中关于皮试的内容。鼓励通过积极反馈,促进修改β内酰胺类抗菌药物说明书中关于皮试的内容。
(三)使用头孢菌素类抗菌药物前,除上述“二、皮试适应证”一节规定的两种需进行皮试的特定情况外,不需皮试。
(四)鼓励医疗机构、相关学术组织等对我国青霉素、头孢菌素过敏反应发生率进行调查,为我国青霉素皮试试剂的最佳组合提供循证医学证据。协调促进研制或引进PPL、MDM,为青霉素皮试提供更完备的试剂种类。
(五)根据世界卫生组织对青霉素皮试的推荐意见,在充分研究,推进修订药品说明书、相关文件、权威著作的基础上:①精准定位青霉素皮试适应证,并从口服青霉素类药物做起,逐步取消常规青霉素皮试筛查;②完善青霉素皮试方法。
(六)医疗机构、相关学术组织和医务人员积极开展面向公众的β内酰胺类抗菌药物皮试知识普及工作,并与相关管理部门充分沟通,为规范β内酰胺类抗菌药物皮试创造良好环境。
(编辑:许男奇 校对:左正荣 审核:王智刚)



【成分】人参(去芦)、酸枣仁、五味子、茯苓、远志、延胡索、天冬、熟地黄、肉桂。
【规格】 6g*10(北京北陆药业)
【价格】 73.91元/盒
【适应症】养心补脾,益气安神。用于广泛性焦虑症心脾两虚证,症见善思多虑不解、失眠或多梦、心悸、食欲不振、精神乏力、头晕、易汗出、善太息、面色萎黄、舌淡苔薄白、脉弦细或沉细。
【用法用量】温开水冲服。早、中、晚各服1袋,一日3次。
【药理作用】 动物试验结果提示:本品可增加焦虑小鼠在明箱停留时间,同时在暗箱停留的时间缩短;增加焦虑大鼠的饮水次数及饮水时的电击次数,增加焦虑大鼠进入高架十字迷宫开臂次数和在开臂停留时间的百分比;可降低焦虑大鼠脑组织中DA、NE的含量,但对5-HT含量无明显影响;可降低小鼠自主活动,延长戊巴比妥钠诱导的小鼠睡眠时间,增加戊巴比妥钠阈下催眠剂量时小鼠的入睡数;延长戊四唑诱发小鼠出现惊厥的潜伏期,降低戊四唑诱发小鼠惊厥的死亡率;延长小鼠断头后喘气维持时间;可不同程度地翻转NE引起的猫血压升高。
【不良反应】偶见口干、视力模糊、便秘增多、恶心呕吐、腹泻、食欲减退或厌食、腹胀、口苦、胃痛、嗜睡、失眠、震颤、头痛、头昏、昏厥、心电图异常、心悸、心动过速、ALT升高、白细胞减少、月经紊乱。
【注意事项】心功能、肝功能异常及白细胞减少者慎用。
【循证依据】
[1]药品说明书:本品于2002年1月由原国家药品监督管理局批准进行临床研究,于2002年7月至2004年8月进行了临床试验,2008年上市。临床试验均采用平行对照、随机、双盲双模拟、多中心临床试验设计方法,观察了九味镇心颗粒用于广泛性焦虑症心脾两虚证的有效性和安全性,对照药为盐酸丁螺环酮片。试验结果显示:Ⅱ期临床试验,九味镇心颗粒组组内治疗前后比较,HAMA总分、HAMA精神性焦虑因子得分、HAMA躯体性焦虑因子得分、中医证候总分变化疗后有改善,差异有统计学意义(P<0.01)。盐酸丁螺环酮片组对HAMA总分、HAMA精神性焦虑因子得分、HAMA躯体性焦虑因子得分、中医证候总分的改善有同样的结果。Ⅲ期临床试验的疗效结果与Ⅱ期临床试验相同。
[2]赵茜;黄娟;吕楠;王学义;詹淑琴;胡永东;毛雪琴;王丽莉;吉恋英;程丽;张玲.九味镇心颗粒治疗广泛性焦虑障碍的效果和安全性[J].中国医药,2022,(07):1070-1073. 选取2012年10月至2014年10月多中心收治的GAD患者209例,采用中央区组随机方法分为2组。对照组(105例)给予帕罗西汀片联合九味镇心颗粒模拟剂治疗,观察组(104例)给予九味镇心颗粒联合帕罗西汀片模拟剂治疗,2组均治疗8周。研究结果显示,治疗后2组HAMA、HAMD-17、SAS总分均低于基线,但2组间比较差异均无统计学意义,说明九味镇心颗粒和帕罗西汀均可改善焦虑症状,治疗第1周起焦虑症状就得到改善,且2种药物对焦虑症状的改善程度相当,本研究治疗8周后2组临床痊愈率和有效率比较差异均无统计学意义。本研究观察组治疗8周期间不良反应发生率低于对照组,2组不良反应均较轻微、患者可耐受,与既往报道结果一致,这可能与九味镇心颗粒对5-羟色胺受体的抑制和拮抗有关。结论九味镇心颗粒对焦虑障碍的躯体化症状、睡眠障碍改善显著,且不良反应少,无药物依赖及戒断反应,且对认知功能无影响。九味镇心颗粒治疗GAD的效果与帕罗西汀片相当,但不良反应发生率低于帕罗西汀片。
[3]范小冬,谢星星,张春燕,向霞,孔文强,杜彪.九味镇心颗粒治疗广泛性焦虑症疗效与安全性的系统评价【J】.成都中医药大学学报,2017,40(02):123-127.该文献是系统评价九味镇心颗粒与坦度螺酮、帕罗西汀、丁螺环酮对照治疗广泛性焦虑症患者的疗效与安全性研究,通过检索,共纳入12篇RCT,合计1407例患者,以疗效肯定的坦度螺酮、帕罗西汀和丁螺环酮为阳性对照组,九味镇心颗粒为试验组,系统评价九味镇心颗粒的疗效和安全性。Meta分析结果显示,九味镇心颗粒与坦度螺酮、帕罗西汀、丁螺环酮显效率(P=0.73)和HAMD评分(P=0.33)差异无统计学意义(P>0.05),可以认为试验组和对照组治疗广泛性焦虑症疗效相当;不良反应方面,对照组发生口干、恶心、心动过速、乏力的危险度分别是试验组的2.0倍、1.7倍、5.3倍、6.7倍,差异有统计学意义。与传统西药相比,九味镇心颗粒治疗广泛性焦虑症疗效上并无显著差异,不良反应也未增加,且在口干、恶心、心动过速及乏力发生率更低。
(编辑:许男奇 校对:左正荣 审核:王智刚)

不同丙戊酸盐和丙戊酸剂型对丙戊酸血药浓度的影响
庄星星,李萌,倪受东,苗仁华(安徽医科大学附属巢湖医院药剂科,安徽巢湖238000)
[摘要]目的:研究不同丙戊酸盐和丙戊酸剂型对丙戊酸血药浓度的影响。方法:回顾性分析某院270例丙戊酸血药浓度监测报告,记录患者姓名、年龄、体质量、丙戊酸的用法与用量、联合用药情况(合用药品及其用法与用量)和血药浓度监测结果。分析不同丙戊酸盐和丙戊酸剂型对丙戊酸标准血药浓度的影响。结果:二元Lo gistic回归分析结果表明丙戊酸盐类型和剂型对标准血药浓度有显著影响(P<0.05);丙戊酸镁的标准血药浓度[(9.18±3.54)μg·kg·mL-1·mg-1]大于丙戊酸钠盐的标准血药浓度[(6.76±2.54)μg·kg·mL-1·mg-1];丙戊酸缓释片的标准血药浓度[(8.38±3.49)μg·kg·mL-1·mg-1]大于丙戊酸普通片的标准血药浓度[(6.88±2.54)μg·kg·mL-1·mg-1],差异均具有显著性(P<0.05)。结论:不同丙戊酸盐和丙戊酸剂型对丙戊酸血药浓度存在明显影响,如何选择丙戊酸盐和丙戊酸剂型对丙戊酸的合理运用具有重要意义。
[关键词]丙戊酸血药浓度;丙戊酸盐;丙戊酸剂型;相关性研究
[中图分类号]R969[文献标识码]A[文章编号]1001-5213(2019)04-0373-04 DOI:10.13286/j.cnki.chinhosppharmacyj.2019.04.13
丙戊酸(valproic acid,VPA)作为临床常用广谱抗癫痫药物,是临床治疗癫痫大发作、小发作以及肌阵挛性发作的首选治疗药物[1-2]。此外,VPA作为目前使用最为普遍的心境稳定剂,用于辅助治疗躁狂症和双相情感障碍等精神疾病。临床实践表明VPA可以有效地治疗躁狂,对双相情感障碍的混合性发作和快速循环发作也具有较好疗效,并能预防其复发[3-5]。
临床医生对丙戊酸钠和丙戊酸镁及其剂型的选择多存在随机和不确定性。笔者通过回顾性分析我院近年来丙戊酸治疗药物监测报道,初步分析丙戊酸盐和丙戊酸剂型对丙戊酸血药浓度的影响,为临床用药提供参考依据。
1资料与方法
1.1临床资料回顾性分析2015年6月至2018年6月期间在我院接受丙戊酸血药浓度监测的270份治疗药物监测报告;收集整理患者姓名、年龄、体质量、丙戊酸的用法与用量、联合用药情况(合用药品及其用法与用量)和血药浓度监测结果等。
为保证研究所需数据的可靠、完整,纳入研究患者均是我院住院患者;接受丙戊酸钠片(0.2g×100片/瓶,湖南湘中制药)、丙戊酸钠缓释片(0.5g×30片/瓶,信东生技股份有限公司),丙戊酸镁片(0.2g×60片/瓶,湖南湘中制药)和丙戊酸镁缓释片(0.25g×30片/盒,湖南湘中制药)治疗;排除肝肾功能异常(肌酐清除率≤50 min·mL-1;ALT或AST≥正常值3倍);以及存在服药依从性问题的病例;排除联合可能影响丙戊酸代谢药物(如苯巴比妥、苯妥英钠以及卡马西平)以及相关数据采集不全的病例。
1.2血样采集和测定所有患者不间断服用丙戊酸至少5d(治疗方案调整后,不间断服药至少3d),于次日清晨服药前采血,监测VPA稳态血药浓度。
VPA血药浓度测定采用HPLC法(A g ilent 1260型高效液相色谱仪,美国安捷伦公司),样本为血清,以环乙烷羧酸为内标物,以2-溴代苯乙酮和三乙胺为衍生化剂,按标准操作规程测定[6]。制备10,40,70,100,130,160μg·mL-1浓度的含药血清,建立标准曲线,计算VPA血药浓度结果。VPA血药浓度参考范围:40~125μg·mL-1(癫痫:40~100μg·mL-1[7];心境稳定剂:50~125μg·mL-1[8];双相情感障碍:77~125μg·mL-1[9])。
为排除身体质量和日服药剂量对丙戊酸血药浓度的影响,将患者的丙戊酸血药浓度监测结果除以每公斤体质量(k g)的日服药剂量(m g),得到标准血药浓度(μg·k g mL-1·mg-1)[10-11]。以标准血药浓度来观察丙戊酸盐和丙戊酸剂型对血药浓度的影响。
1.3统计学处理应用SPSS 21.0统计学软件处理数据,计数资料以x±s表示,组间数据比较采用t检验。采用Logistic进行回归分析,考察相关性。P<0.05表示差异有显著性。
2结果
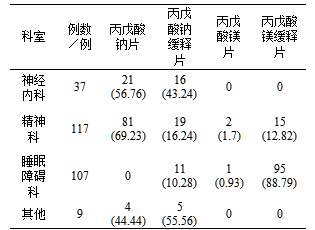
2.1临床科室对丙戊酸制剂使用情况纳入研究270份治疗药物监测报告,其中神经内科37份,精神科117份,睡眠障碍科107份,其他临床科室9份。总体上,丙戊酸钠盐157份(58.15%)丙戊酸镁盐113份(41.85%);丙戊酸普通片109份(40.37%)丙戊酸缓释片161份(59.63%)。
神经内科37份均为丙戊酸钠盐,普通片和缓释片分别为21份(56.76%)和16份(43.24%)。精神科117份监测报告中,丙戊酸钠盐100份(85.47%)丙戊酸镁盐17份(14.53%);普通片83份(70.94%)缓释片34份(29.06%)。睡眠障碍科107份监测报告,其中丙戊酸钠盐11份(10.28%)丙戊酸镁盐96份(89.72%);普通片1份(0.93%)缓释片106(99.06%)。其他临床科室共9份,均为丙戊酸钠盐,普通片和缓释片分别为4份(44.44%)和5份(55.56%)。详见表1。
表1临床科室各丙戊酸制剂和丙戊酸盐使用情况[例(%)]
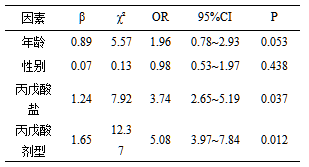
2.2 Lo g istic回归分析以标准血药浓度为因变量,以年龄、性别、剂型和丙戊酸盐类型为自变量,采用二元Lo g istic回归分析影响因素。结果表明丙戊酸盐类型和剂型对标准血药浓度有显著影响(P<0.05),详见表2。
表2二元Lo gistic回归分析结果
2.3丙戊酸钠和丙戊酸镁与丙戊酸血药浓度的相关性丙戊酸钠盐和丙戊酸镁盐的平均血药浓度分别为(70.16±19.69)μg·mL-1和(67.74±21.10)μg·mL-1,无显著性差异;丙戊酸钠盐的标准血药浓度(6.76±2.54)μg·kg·mL-1·mg-1小于丙戊酸镁盐的标准血药浓度(9.18±3.54)μg·kg·mL-1·mg-1,差异有显著性(P=0.012),见表3。
表3丙戊酸钠和丙戊酸镁与丙戊酸血药浓度的相关性(x±s)
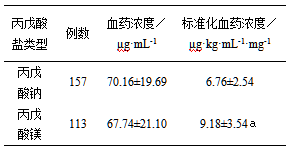
注:丙戊酸钠和丙戊酸镁组相比,差异有显著性(a P<0.05)
以标准血药浓度为X轴,出现频率(%)为Y轴作正态分布图(图1);
由图可知,丙戊酸镁盐的标准血药浓度正态分布图较丙戊酸钠盐沿X轴右移。丙戊酸钠盐的标准血药浓度正态分布图Skewness系数0.75,Kurtosis系数0.36;丙戊酸镁盐的标准血药浓度正态分布图Skewness系数1.17,Kurtosis系数1.64;2种丙戊酸盐的标准血药浓度正态分布图都呈现右偏态(Skewness系数大于0)其中丙戊酸镁的标准血药浓度正态分布图尾部存在大数据分布(Kurtosis系数大于1)。说明丙戊酸镁盐标准血药浓度大于丙戊酸钠盐,丙戊酸镁盐的血药浓度比丙戊酸钠盐更集中,稳定。

标准血药浓度/μg·kg·mL'·mg'
A.丙戊酸钠盐;B.丙戊酸镁盐
图1丙戊酸钠盐和丙戊酸镁盐的标准血药浓度正态分布图
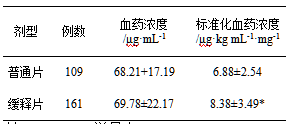
2.4丙戊酸普通片和丙戊酸缓释片与丙戊酸血药浓度的相关性研究丙戊酸普通片和丙戊酸缓释片的平均血药浓度分别为(68.21±17.19)μg·mL-¹和(69.78±22.17) μg·mL-¹,差异无显著性;丙戊酸普通片的标准血药浓度(6.88±2.54)μg·kg·mL-¹·mg⁻¹,丙戊酸缓释片的标准血药浓度(8.38±3.49)μg·kg·mL-¹·mg-¹,差异具有显著性(P=0.029),详见表4。
表4丙戊酸片和丙戊酸缓释片与丙戊酸血药浓度的相关性(±s)
注:丙戊酸钠组和丙戊酸镁组相比,差异有显著性(&P<0.05)
以标准血药浓度为X轴,出现频率(%)为Y轴作正态分布图(图2)。如图所示,缓释片的标准血药浓度正态分布图较普通片沿X轴右移。丙戊酸普通片的标准血药浓度正态分布图Skewness系数0.78,Kurtosis系数0.68;丙戊酸镁盐的标准血药浓度正态分布图Skewness系数1.13,Kurtosis系数1.77;2种丙戊酸剂型的标准血药浓度正态分布图都呈现右偏态(Skewness系数大于0)其中缓释片的标准血药浓度正态分布图尾部存在大数据分布(Kurtosi s系数大于1)。说明丙戊酸缓释片的标准血药浓度大于普通片,缓释片的标准血药浓度的分布区间更集中。
3讨论
3.1临床科室的用药选择丙戊酸盐的类型和丙戊酸剂型选择与丙戊酸的临床疗效密切相关。临床研究资料表明丙戊酸镁盐的抗癫痫和抗惊厥药优于丙戊酸钠盐[12];丙戊酸缓释制剂由于可以提供稳态的药物浓度,其临床疗效也是优于普通片剂[13]。
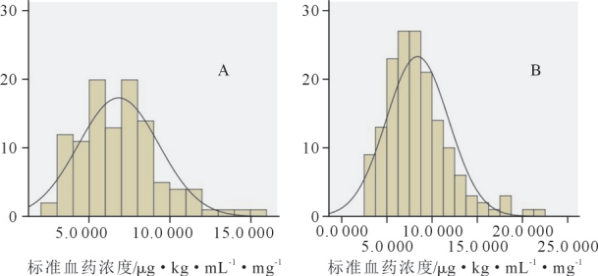
标准血药浓度/μg·kg·mL¹·mg;
A.丙戊酸片剂;B.丙戊酸缓释片
图2丙戊酸片剂和丙戊酸缓释片的标准血药浓度正态分布图
本研究中发现临床科室对丙戊酸盐和丙戊酸剂型的选择多存在不确定性和随机性或习惯用药。低年资医师多根据高年资医师的用药习惯选择用药。这些都导致临床上在丙戊酸盐和丙戊酸剂型选择上的一些不合理。如表1所示神经内科37份丙戊酸治疗药物监测报告中,均为丙戊酸钠盐,多数临床研究已证实丙戊酸镁的抗癫痫疗效要优于丙戊酸钠盐,且不良反应少。多数学者都推荐在治疗难治性癫痫时,使用丙戊酸镁盐代替丙戊酸钠盐。丙戊酸作为心境稳定剂辅助治疗精神类疾病时,一方面要求维持较高的稳态血药浓度水平,另一方面为了提高服药依从性,尽量减少服药频次。然而我院精神科普通片的使用率为70.94%,能够缓慢释药,提高稳态药物浓度水平,减少患者服药频次的缓释片的使用率仅为29.06%。笔者认为,在医院药学服务转型的新形势下,临床药师应有效地利用药学专业知识,为临床选择用药提供合理的建议,才能提高医院合理用药水平。
3.2丙戊酸钠盐和丙戊酸镁盐丙戊酸可以增加GABA的水平,增强GABA的活性,降低神经元兴奋性,临床用于多种类型的癫痫治疗以及作为心境稳定剂用于精神疾病的辅助治疗。目前临床运用的主要是钠盐和镁盐2种丙戊酸制剂,两者的临床作用基本相同。近年来,部分学者研究发现丙戊酸镁在抗癫痫和抗惊厥的临床疗效均优于丙戊酸钠[14-16]。本研究也发现丙戊酸镁盐的丙戊酸标准血药浓度显著高于丙戊酸钠盐,说明丙戊酸镁在临床使用时,可以提供更有效的稳态血药浓度,该发现与临床报道相符。
3.3丙戊酸普通片和丙戊酸缓释片与丙戊酸普通片剂相比,缓释片具有以下优势:(1)可以减少给药的次数,提高患者服药依从性;(2)明显减小血药浓度曲线峰谷波动,使血药浓度平稳;(3)避免普通片剂快速溶解释放药物,对胃肠道引起的刺激[17-18]。药动学研究显示丙戊酸镁缓释片中的丙戊酸镁在大鼠体内的tmax为7 h,给药后1~6 h丙戊酸血药浓度缓慢上升,7 h左右达峰值,药物浓度维持在400 n g·mL-1以上时间长达80 h。而丙戊酸镁片在给药后1 h内血药浓度快速上升,1~2 h达到高峰,4 h以后下降明显,直至全部消失[19]。说明缓释片可以提供更高、更稳定的药物浓度。这与本研究得到的结果相吻合。临床资料显示服药依从性问题都普遍存在于癫痫和精神疾病患者中,丙戊酸缓释片可以减少服药频次,提高血药浓度,对提高患者服药依从性和临床疗效都大有益处[20-23]。笔者认为丙戊酸的缓释制剂更应该在临床推广使用。
综上所述,丙戊酸镁和丙戊酸缓释片更值得在临床上推广。
(编辑:曹雅茹、许男奇 校对:左正荣 审核:王智刚)

盘点!那些导致QT间期延长的抗精神病药物及分层管理
长 QT 综合征(Long QT syndrome,LQTS)在心电图上表现为 QT 间期延长,易合并尖端扭转性室速、室颤等恶性心律失常,导致猝死。LQTS 可分为先天性 LQTS 和获得性 LQTS,而获得性 LQTS 主要由比如低钾,低镁血症,以及各种导致 QT 间期延长的药物引起,而大部分抗精神病药物可不同程度地影响QT间期,机制主要为阻断钾离子通道;当QT间期>500ms时,尖端扭转型室性心动过速的发生风险显著升高。
一、抗精神病药对QT间期的影响
抗精神病药物对QT间期的影响
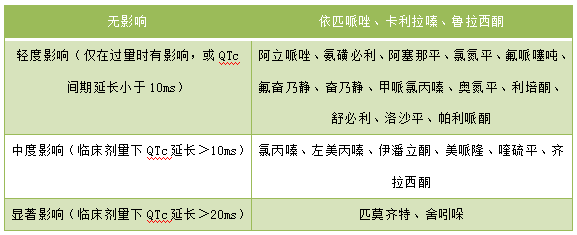
目前认为仅有的三种不延长QT间期的抗精神病药为鲁拉西酮、卡利拉嗪及依匹哌唑。若患者的QTc间期(校正后QT间期)显著延长,如>500ms,且无其他可逆转的病因(如未联用其他可延长QT间期的药物),此时原则上应换用上述三种药物之一。然而,更换抗精神病药可能带来精神病复发风险的轻度升高;从氯氮平换用其他抗精神病药时,复发风险可能尤高。
二、QTc间期延长的分层应对策略
不同QTc间期下的管理策略

若患者存在T波异常,则应回顾现有治疗;此时可考虑降低抗精神病药剂量,或换用对QT间期影响较小的药物,如鲁拉西酮、卡利拉嗪或依匹哌唑。
三、评估要点
心内科/电生理评估内容应包括心电图、超声心动图、24小时动态心电图、电解质监测及肝功等。若发现患者存在冠状动脉性心脏病(CHD)的证据,NICE指南建议完善冠脉造影。
应评估精神科药物之外的其他潜在可逆因素,包括生理因素。例如,与低钾血症相关的QTc间期延长更常见于因急性精神病发作入院的患者。
QTc间期延长及心律失常的生理学高危因素

联用药物因素也需要考虑:
一般情况下,一种尖端扭转型药物与另一种尖端扭转型药物是有使用禁忌的,当然也有一些例外,但是不建议同时使用,如必须联用,需密切加强心血管毒性症状监测。然而以下这些药物没有例外,西酞普兰、依地普仑、多潘立酮、羟嗪和哌喹与所有的尖端扭转型药物禁忌。
针对我院现有精神科药物,建议如氯丙嗪、喹硫平、齐拉西酮等对QT间期有中度影响的药物,与其他影响延长QT间期的药物应避免联合使用,氨磺必利、利培酮、舒必利等对QT间期有轻度影响的药物,与其他轻度影响延长QT间期的药物应谨慎联合,必要时需密切加强心血管毒性症状监测。
某些非精神科药物可延长QT间期,β2受体激动剂及拟交感药可能在QTc间期延长者中诱发尖端扭转型室性心动过速。

另一方面,药物对QT间期的影响往往呈血药浓度依赖性,因此药物相互作用也很重要。一些药物可抑制抗精神病药的代谢,升高后者的血药浓度,如氟伏沙明、氟西汀、帕罗西汀及丙戊酸盐等,临床中须警惕。如果未发现抗精神病药之外的可逆高危因素,则可能需要考虑更换抗精神病药。
患者自身因素也需要考虑。例如,用药后出现QT间期显著延长的患者中,很大一部分人本身即存在离子通道突变。针对这一情况,可考虑停药至少5个半衰期后评估有无复极化异常,或分析患者的家族史,如家人有无年轻时即猝死、婴儿猝死、癫痫、先天性耳聋等情况,以评估遗传性通道病变的可能。如有必要,完善离子通道突变检测。
需要指出的是,其他心血管高危因素,如吸烟、肥胖及糖耐量异常等,对患者基本状况的不利影响远远超过了具有不确定性的QT间期延长本身,同样需要加以评估及管理。
对于所有使用抗精神病药的患者,均应在入院时及出院前完善心电图及QT间期检查,此后每年复查心电图。
参考文献:
[1]2019 BHRS临床实践指南:抗精神病药物导致QT间期延长患者的管理
[2]药品说明书
(编辑:朱亚男 校对:左正荣 审核:王智刚)

EMA修改选择性5-羟色胺再摄取抑制剂、5-羟色胺-去甲肾上腺素再摄取抑制剂等的产品信息警示产后出血风险
2020年10月26日,欧洲药品监督管理局(EMA)发布消息,修改西酞普兰(citalopram)、去甲文拉法辛(desvenlafaxine)、艾司西酞普兰(escitalopram)、氟西汀(fluoxetine)、氟伏沙明(fluvoxamine)、米那普仑(milnacipran)、帕罗西汀(paroxetine)、舍曲林(sertraline)、文拉法辛(venlafaxine)、沃替西汀(vortioxetine)的产品信息,警示产后出血风险。
EMA药物警戒风险评估委员会(PRAC)综合考虑了出血事件与选择性5-羟色胺再摄取抑制剂(SSRIs)、5-羟色胺-去甲肾上腺素再摄取抑制剂(SNRIs)、沃替西汀之间的已知关联性,以及关于孕妇使用抗抑郁药,特别是SSRIs和SNRIs,发生产后出血的部分观察性研究结果。根据证据审查结果,米氮平、曲唑酮、阿米替林和安非他酮(包括其与纳曲酮的组合)的产品信息暂不要求更新;阿米替林(Lundbeck)原研上市许可持有人(MAH)需在下一个PSUSA(PSUR single assessment)程序中监测出血和产后出血事件;度洛西汀目前已达成一致的措辞足以提示上述风险。
PRAC审议了原研MAH对措辞的意见以及对产后出血事件发生频率的讨论,同意含西酞普兰、去甲文拉法辛、艾司西酞普兰、氟西汀、氟伏沙明、米那普仑、帕罗西汀、舍曲林、文拉法辛产品的MAH在PRAC建议发布后的2个月内提交变更,按如下要求修改产品信息(带下划线的部分为此次新增内容):
产品特性概要
1.使用时的特别警告和注意事项
SSRIs/SNRIs可能增加产后出血的风险。
2.生育、怀孕和哺乳
观察数据表明,在分娩前一个月内暴露于SSRI/SNRI会增加产后出血的风险(小于2倍)。
3.不良反应
SOC生殖系统与乳房疾病:产后出血*;频率未知
在不良反应表下添加产后出血属于类效应(class effect)的注释:*此事件在SSRIs/SNRIs治疗类别中已有报告。
4. 服药前需要了解的内容
警告和注意事项:
在使用本品之前,请先咨询医生,尤其如果有以下情况:
出血性疾病史或怀孕;如果在怀孕快要结束时使用本品,则分娩后不久发生阴道大出血的风险可能增加,特别是如果有出血性疾病史。应告知医生或助产士您正在使用本品的消息,以便他们为您提出建议。
4. 可能的副作用
频率未知:分娩后不久阴道大出血(产后出血)。
(欧洲药品管理局EMA网站)
(编辑:朱亚男 校对:左正荣 审核:王智刚)
附:
市四院国家、长三角及省集采药品目录(2023年)
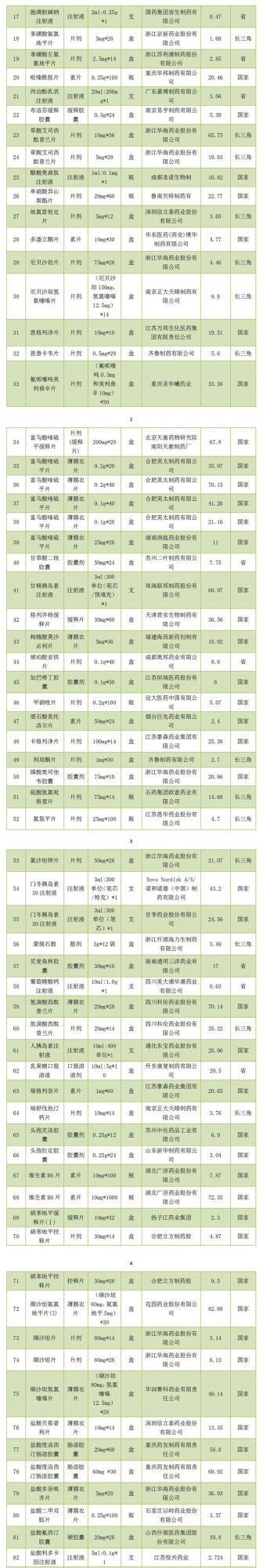
(编辑:许男奇 校对:左正荣 审核:王智刚)
